BIO – Medicina Costruzione Sociale nella Post-Modernità – Educational Papers • Anno IX • Numero 36 • Dicembre 2020
La promessa fatta alla medicina convenzionale dalla finestra della nanoscala
Nell’ambito delle ricerche in nanotecnologie stanno postulando che a livello del minuscolo, la biologia sia tutta una questione di ingegneria e che per questa ragione la nanotecnologia possa rinnovare la medicina dall’interno. Contestare, confutare o invece riconoscere un tale approccio con proprietà richiede, al minimo, competenze circa quali siano le condizioni sotto le quali si possa avere conoscenza sia in medicina che in fisica, biologia e nanotecnologie e, inoltre, competenze medico-cliniche. Lungi da me, semplice sociologo curatore della presentazione dell’argomentazione, poter affrontare un’impresa simile. Le implicazioni di una tale promessa nella costruzione dell’immaginario sociale mi obbligano, invece, in qualità di responsabile di una testata che si occupa di gettare luce proprio nel Retroscena della Costruzione Sociale della Medicina, ad esplorare questa promessa prometeica con le sue metafore meccanicistiche.
Il campo di ricerca e riflessione è, senza dubbio, importante e, riconoscendo la sua rilevanza, va seguito, approfondito e divulgato. Ed è questo il proposito e limite di questa relazione nella quale cerco di sintetizzare le idee sullo stato dell’arte dell’intersezione della ricerca tra fisica, biologia, nanotecnologie e medicina, seguendo uno dei ricercatori più affermati nel campo, Sonia Contera, attraverso le sue argomentazioni apparse nel suo libro Nano Comes to Life: How Nanotechnology Is Transforming Medicine and the Future of Biology, pubblicato dalla Princeton University Press, lo scorso ottobre del 2019.1
Storia della promessa: lo studio della materia a scala nanometrica
A metà degli anni ’80, dai laboratori interessati alla questione iniziarono ad emergere evidenze che confermavano che gli studiosi erano finalmente in grado di raggiungere il livello nanometrico in condizioni sperimentali e non solo con le loro teorie. Lavorando su scale definite in milionesimi di millimetro, Richard Smalley, Robert Curl e Harold Kroto relazionarono la loro scoperta del “buckminsterfulleren”2, vale a dire un poliedro di dimensioni nanometriche, con 32 facce fuse in una struttura a forma di palla da calcio e con atomi di carbonio in ciascuno dei suoi 60 vertici.
Queste “buckminsterfullerene” o palline in miniatura, chiamate in questo modo per la loro somiglianza con le strutture a cupola geodetica realizzate dall’architetto Richard Buckminster Fuller negli anni ’50, si trovano in piccole quantità nella fuliggine, nello spazio interstellare e nelle atmosfere di stelle giganti rosse ricche di carbonio, ma Kroto è stato in grado di ricrearle in reazioni chimiche in laboratorio durante le sue visite accademiche alla Rice University in Texas. Nel 1991, il laboratorio del rinomato esperto in materia di nanotecnologie, Nadrian C. Seeman, presso la New York University, ha utilizzato 10 filamenti artificiali di DNA per creare3 la prima nanostruttura tridimensionale prodotta dall’uomo, collegando i filamenti di DNA per assomigliare ai bordi di un cubo, segnando così l’inizio del campo ora noto come “Nanotecnologia del DNA”. Alcuni ricercatori, con ampie visioni, iniziarono a rendersi conto che un nuovo tipo di tecnologia, profetizzato da Richard Feynman negli anni ’50, si stava finalmente materializzando, nella misura in cui loro raggiunsero la capacità di visualizzare, fabbricare e manipolare la materia su scala nanometrica.
Il termine nanotecnologia è stato coniato nel 1974 dallo scienziato giapponese Norio Taniguchi per descrivere quel campo nel quale si possono manipolare materiali ad un livello estremamente fine e minuto, in particolare per descrivere i processi dei semiconduttori che coinvolgono l’ingegneria su scala nanometrica ma è entrato nel dibattito pubblico solo con la pubblicazione nel 1986 dell’influente Engines of Creation, The coming Era of Nanotechnology di K Eric Drexler iperbolico libro di scienza futuristica che immaginava ciò che potrebbe essere ottenuto sulla scala dell’inimmaginabilmente piccolo. Il libro di Drexler ha suscitato polemiche durature, in particolare incentrate sulle deboli basi scientifiche di alcune delle sue idee ma niente si attaccò di più all’immaginario sociale della sua previsione di un ipotetico “grey goo”4, flagello di una distopia globale che coinvolgeva macchine auto-replicanti fuori controllo che divoravano tutta la vita sulla Terra.
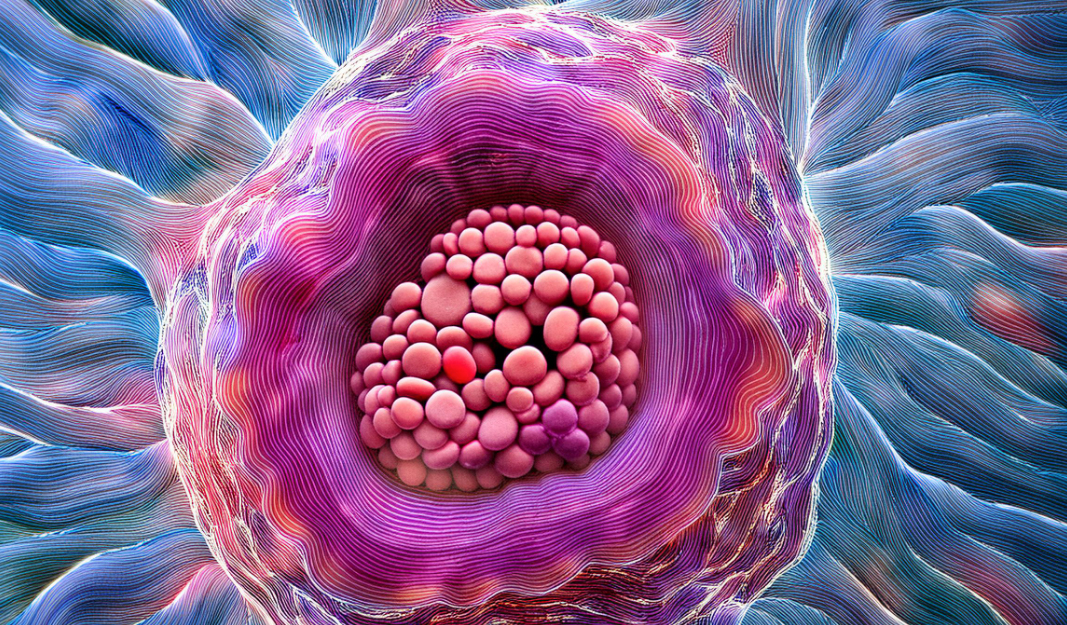
Forse il punto di svolta principale nel passaggio della nanotecnologia dalla teoria alla realtà è stato lo sviluppo del microscopio a effetto tunnel (the scanning tunnelling microscopie – STM), una macchina ingegnosa che ha aggirato i limiti dei microscopi convenzionali, basati sulla luce, interagendo con le nanostrutture con l’utilizzo di una punta molto affilata, sottile quanto un singolo atomo. Scansionando la punta atomica sul campione, in modo molto controllato, e mappando le interazioni locali della punta con l’esterno del campione, si poteva creare un’immagine che delineava la sua superficie con precisione atomica. Con l’STM, che nel 1986 è valso ai suoi inventori, Gerd Binnig e Heinrich Rohrer, il Premio Nobel per la Fisica, i singoli atomi sono diventati “visibili” o, più precisamente, “percepibili” nel modello di raffigurazione. Ma oltre all’imaging con una precisione senza precedenti, utilizzando uno strumento relativamente semplice ed economico, l’STM aveva capacità drasticamente nuove: era in grado di raccogliere e disporre gli atomi uno per uno.

L’immagine sopra rende un’idea della svolta che significò nello studio della materia l’utilizzo del microscopio a effetto tunnel (the scanning tunnelling microscopie – STM). Infatti, nell’immagine possiamo vedere un’onda stazionaria che appare al centro del cerchio completato fatto di atomi. L’ondulazione è prodotta da un’onda di elettroni che emerge all’interno del recinto quantistico. Questa è una visualizzazione meravigliosa della meccanica quantistica (particelle che si comportano come onde) e riassume, efficacemente, lo stato dello studio della materia negli anni ‘90. In quanto strumento riduzionista, l’STM potrebbe spostare e costruire materia usando singoli atomi come mattoni e, allo stesso tempo, rappresentare un fenomeno ondulatorio complesso che emerge come risultato e che può essere spiegato solo dalle teorie della materia che insistono sul fatto che “il tutto è più grande delle parti”.
Storia della promessa: lo studio della materia a scala nanometrica e la svolta verso la biologia
Negli anni ’90, alcuni ricercatori del mondo della fisica su scala nanometrica hanno iniziato a portare la loro esperienza verso la biologia. Fin dall’inizio, i nanotecnologi sono stati coinvolti e ispirati dalla biologia, principalmente perché gli attori molecolari e i principali bersagli farmacologici in medicina – proteine, DNA e altre biomolecole – sono nanometrici. Ma i fisici erano anche affascinati dalla capacità della biologia di produrre materiali che si adattano, si evolvono, sopravvivono e persino “pensano” – materiali che superano le capacità tecnologiche umane in ogni modo possibile.
Alcuni dei fisici di allora impegnati nello sviluppo delle nanotecnologie erano interessati a come nell’Universo si fosse sviluppato e a ciò che viene culturalmente chiamato vita utilizzando molecole allungate, simili a stringhe (polimeri), in grado di piegarsi in una miriade di nano-forme (proteine) che si assemblano in tutti gli organismi viventi che esistono sulla Terra. Gli strumenti della nanotecnologia hanno permesso, per la prima volta, agli studiosi di indagare, a livello molecolare, i meccanismi fisici che rendono possibile la vita. In particolare, potevamo esplorare come la meravigliosa complessità della biologia sia sostenuta dal comportamento dinamico di quelle “nanomacchine” biologiche che chiamiamo proteine.
Negli ultimi 30 anni, i nano-microscopi (principalmente il microscopio a forza atomica o AFM, un parente stretto dell’STM) hanno rivelato come le proteine estraggono energia dall’ambiente e svolgono i compiti necessari per mantenere in vita un organismo. Lungi dall’essere entità statiche, presenti nei tradizionali libri di biochimica, le proteine sono state osservate eseguire movimenti complessi ma sorprendentemente familiari che, a volte, hanno una strana somiglianza con macchine macroscopiche di fabbricazione umana. Alcune funzionano come nano-motori che ruotano per massimizzare l’efficienza delle reazioni chimiche, altre possono “camminare” su binari molecolari con un movimento processivo “mano su mano” che consente loro di trasportare carichi intorno alla cellula.
La nanomedicina: tra clamore e fallimento
Con i suoi avanzamenti, la nanotecnologia ha posto la sua massima attenzione, anziché verso la ricerca della fisica riguardo la materia oppure verso la complessità in sé della biologia, su un’area di ricerca che dovrebbe portare a ricompense più tangibili: quella di migliorare l’efficacia dei trattamenti medici, specialmente nella chemioterapia del cancro. Nei protocolli convenzionali, uno dei requisiti principali affinché un farmaco sia considerato efficace è che deve raggiungere i suoi obiettivi molecolari in concentrazioni sufficientemente elevate. Il problema con la chemioterapia, però, è che è molto difficile concentrare i farmaci nel sito del tumore, da qui le dosi molto alte e tossiche impiegate. Negli anni ’80, i ricercatori hanno scoperto che le nanoparticelle si accumulavano in alcuni tumori a causa della particolare struttura dei loro vasi sanguigni, il che ha portato a grandi speranze nell’utilizzo di nanostrutture per migliorare la somministrazione di farmaci alle cellule cancerose. Il campo, immediatamente soprannominato “nanomedicina“, è cresciuto rapidamente. Ma le aspettative non sono state all’altezza del clamore: attualmente meno di 20 nanomedicine sono state approvate per l’uso nel trattamento del cancro. La ricerca di proiettili magici a nanotecnologia e di scorciatoie fortunate per curare le malattie, pur trascurando la complessità della biologia coinvolta, non si è dimostrata particolarmente fruttuosa. Rispecchiando le strategie della farmacologia, la nanomedicina ha ampiamente riprodotto i suoi fallimenti.
Nella seconda metà del XX secolo, lo studio delle molecole biologiche e della loro chimica si era già trasformato in una ricerca sempre più strutturale, rendendo la biologia stessa un tentativo riduzionista di spiegare il tutto sommando le sue parti. Questa tendenza è stata stimolata dagli sviluppi tecnologici che hanno portato alla scoperta del cosiddetto macchinario molecolare della vita. A metà del secolo, ad esempio, gli studiosi sono stati in grado di risolvere le strutture dettagliate delle biomolecole utilizzando i raggi X su cristalli colloidali5 di biomolecole estratte dal loro ambiente naturale.
Allo stesso tempo, i progressi nella genetica e nella biochimica hanno portato a una maggiore comprensione dell’attività chimica delle proteine e della loro relazione con le informazioni immagazzinate nel DNA cellulare. Gli studiosi sono stati incoraggiati a sviluppare un’interpretazione della biologia che tentasse soluzioni semplici alla sua scoraggiante complessità. Di conseguenza, hanno visto gli organismi viventi come computer biochimici che eseguono un programma molecolare. E hanno visto quel programma come un algoritmo codificato in geni e materializzato da proteine. In questo quadro, i ricercatori medici si sono concentrati sull’identificazione dei geni e delle proteine canaglie che avrebbero causato malattie e sulla ricerca di farmaci per disattivarli. Il problema con questo approccio riduzionista sarebbe che esso, a quanto pare, non considera come cellule gli organi e i tumori. Gli organismi biologici si intrecciano con il loro ambiente, combinandosi e ricombinandosi e utilizzando collettivamente le loro strutture su ogni scala (dal nanometro al metro e oltre) per continuare a sopravvivere, vivere ed evolversi.
Per essere onesti, l’approccio riduzionista al trattamento delle malattie è stato giustificatamente alimentato per decenni da scoperte rivoluzionarie di farmaci – antibiotici, chemioterapia e altri “farmaci miracolosi” – che hanno portato a notevoli miglioramenti nell’aspettativa di vita. Tuttavia, questo secolo XXI ha visto un forte calo del numero di nuovi farmaci efficaci prodotti. Tra il 2002 e il 2014 sono comparsi in totale 71 nuovi farmaci antitumorali, di cui solo 30 – ritenuti in grado di prolungare la vita in pazienti con tumori solidi in media di 2,1 mesi, rispetto ai farmaci più vecchi – hanno ottenuto l’approvazione dalla Food and Drug Administration statunitense . I costosi e, in gran parte, inefficaci metodi per tentativi ed errori (trail-and-error methods) utilizzati per identificare nuovi farmaci e la difficoltà di condurre studi clinici (clinical trails) sono stati in parte responsabili di questa svolta al ribasso.
Più significativa, tuttavia, è stata la capacità degli organismi biologici di evolvere resistenza a nuovi trattamenti. La resistenza agli antibiotici è ora ampiamente identificata6 come una delle maggiori minacce per la salute pubblica. Nel frattempo, la capacità delle cellule tumorali di costruire difese contro la chemioterapia ha bloccato i farmacologi alla ricerca di cure contro il cancro. I batteri e il cancro ci stanno insegnando la stessa lezione che stiamo imparando in altri aspetti del nostro rapporto con la natura: vale a dire che la vita “resiste” agli approcci riduzionisti e si riprende con comportamenti complessi che ostacolano le nostre strategie ottimistiche per dominarla.
La meccanica quantistica ha svelato una realtà più complicata di quanto avessimo immaginato
Negli ultimi due decenni, sia la medicina sia la biologia hanno affrontato questioni che gli approcci intellettuali e la compartimentalizzazione delle discipline prevalenti nel XX secolo non potevano risolvere. In questo senso, la nanotecnologia è arrivata al momento giusto, ispirando una nuova generazione di fisici e ingegneri a volgere lo sguardo verso la biologia. I pionieri generalmente cercano nuovi modi di fare le cose, sfuggendo alle istituzioni conservatrici dell’establishment per costruire nuove realtà, e così è stato con la nuova generazione di fisici, biologi e ingegneri impegnati con le nanotecnologie. Tediati dal dogmatismo che domina la biologia molecolare, hanno messo in dubbio i suoi modelli riduzionisti riguardo alla vita e alla malattia. La loro educazione ha fornito loro gli strumenti della matematica, la capacità di costruire macchine per interrogare la materia e il desiderio di collaborare con studiosi dei materiali, consentendo loro di creare nuove applicazioni per trasformare il panorama medico e tecnologico. Fondamentalmente, i fisici portavano il bagaglio storico di un campo che, per la maggior parte di un secolo, era stato continuamente costretto a rivedere le sue teorie fondamentali per interpretare la realtà. In fisica, nulla è stato risolto a lungo. Il successo della relatività generale e della meccanica quantistica ha rivelato una realtà molto più meravigliosa e incomprensibilmente complicata di quanto avessimo osato immaginare. Chi potrebbe dire cosa potrebbe accadere se la biologia fosse soggetta a rivoluzioni simili?
Si consideri, per un momento, come è stata trasformata la fisica, dal concentrarsi su come i singoli elementi (atomi, pianeti) hanno interagito tra loro, al preoccuparsi di cosa succede quando molti elementi interagiscono tra loro – atomi nei solidi, molecole nell’acqua – e a riflettere su come apparentemente modelli di comportamento non correlati emergono da queste interazioni. Il comportamento macroscopico, quale i materiali superconduttori o magnetici, è stato in questo modo spiegato da concetti astratti che estraggono l’essenza di come le interazioni collettive tra gli atomi diano luogo a comportamenti più semplici su scale più grandi (ad esempio, magneti che si attraggono a vicenda). Allo stesso modo, la fisica della materia morbida è stata in grado di prevedere il comportamento meccanico di grandi pezzi, diciamo, di gomma, dalle interazioni dei suoi componenti molecolari, uno sviluppo che ora viene sfruttato nella progettazione di scarpe da corsa e pneumatici ad alta tecnologia.
Infatti, grazie alla fisica moderna (vale a dire fisica atomica, fisica nucleare e subnucleare, fisica delle particelle, astrofisica e cosmologia), alcuni studiosi hanno continuato a scoperchiare ulteriormente come la natura usi la complessità per creare gli strati che compongono la nostra realtà, dal bosone di Higgs al comportamento di uno stormo di uccelli. Le regole della trasformazione da semplice a complesso, complesso che poi emerge nuovamente in comportamenti più semplici, sono, come nel caso della gomma, misurabili e modellabili con la matematica. Sebbene la biologia sia immensamente più complicata della gomma, per non dire che siamo molto lontani dallo spiegare la coscienza o l’emozione con la matematica, niente ostacola i fisici che cercano di testare i limiti della nostra comprensione della realtà e immaginano cosa si possa fare con quella conoscenza.
La fisica moderna e la costruzione di nuove realtà: la nanotecnologia delle proteine
Un campo emergente che esemplifica questa trasformazione della scienza è la “nanotecnologia proteica”, in cui i nanotecnologi utilizzano le proteine7 per progettare e costruire microstrutture e nanostrutture, “imitando” così la “vita”. Le proteine sono considerate, metaforicamente, i mattoni della vita. In natura, risultano dal ripiegamento attento e deterministico di stringhe molecolari (polimeri) costituite da combinazioni di 20 unità differenti (amminoacidi). Possono assumere qualsiasi forma e funzione immaginabile su nanoscala. In realtà, non sappiamo ancora quante proteine diverse ci sono nel nostro corpo (forse è qualcosa di inconoscibile), poiché le nostre cellule potrebbero avere la capacità di creare e modificare le proteine quando ciò si rende necessario. Le proteine funzionano come rilevatori di luce nei nostri occhi, interruttori elettrici nei nostri neuroni, nano-walker nei nostri muscoli e nano-motori rotanti per catalizzare le reazioni chimiche. Sono altresì responsabili di rilevare e reagire ai segnali, alle forze e alle informazioni dall’ambiente in cui risiede un organismo e, ugualmente, di creare le strutture che consentono il movimento, l’estrazione di energia dal cibo o la distruzione di agenti patogeni. Nessuna nanotecnologia artificiale creata dall’uomo può sognare tali capacità, ma possiamo provare a imparare come lo fa la vita.
I nano-tecnologi delle proteine sono stati ispirati dal recente successo degli studiosi che hanno cercato a lungo di risolvere uno dei più spinosi rebus della biologia molecolare: prevedere la forma di una proteina data l’informazione sulla composizione della sua catena di amminoacidi, informazione che allo stato dell’arte delle tecnologie risulta relativamente facile da ottenere. Per anni, il problema della previsione è stato considerato troppo difficile perché la complessità delle interazioni tra gli amminoacidi della proteina significava che le loro forme emergenti erano impossibili da calcolare con la capacità limitata dei computer di una volta.
Il primo chiaro successo nel prevedere, correttamente, una struttura proteica è arrivato nel 2014, da un team guidato da David Baker presso l’Università di Washington. Due fattori importanti possono essere individuati nello spingere questo risultato. Il primo è stato il crowdsourcing: il team di Baker ha calcolato con successo la forma corretta della proteina sfruttando le risorse di elaborazione dati di migliaia di volontari e i loro personal computer. Il secondo fattore era rendersi conto che le interazioni dei mattoni da sole non erano sufficiente: le strutture proteiche corrette potevano essere inferite solo tenendo conto della loro storia evolutiva. Questa era una svolta radicale dal modo in cui le cose erano state fatte prima. Per comprendere la fisica della biologia e, quindi, per costruire strutture come fa la biologia, “la storia evolutiva della vita sulla Terra deve essere inclusa nei calcoli matematici.”
Questa consapevolezza è venuta dalla scoperta fatta ad Harvard da Chris Sander e Debora Marks dalle “graffette” strutturali (formate da amminoacidi che si attaccano tra loro) che tengono insieme una molecola proteica. Sanders e Marks hanno esaminato le informazioni contenute nel DNA genomico di organismi che hanno proteine correlate tra loro attraverso una storia evolutiva condivisa. Quando le “graffette strutturali di base” vengono inserite nel modello del computer, è possibile esplorare come la proteina si ripiega entro questi vincoli. La strategia, in altre parole, trasforma un problema impossibile in uno calcolabile. A differenza delle strutture inerti dei magneti, l’evoluzione guida la complessità in biologia, selezionando le forme e le funzioni che consentono la sopravvivenza.
Una volta che gli studiosi sono riusciti a prevedere la struttura delle proteine, hanno immediatamente iniziato a utilizzare le idee per creare “proteine progettate” che non esistevano in natura e ad applicarle a scopi medici e tecnologici specifici. Per fare questo hanno dovuto hackerare il meccanismo molecolare delle cellule microbiche viventi (principalmente batteri o cellule di lievito) e poi riprogettarle “per produrre” le proteine che hanno progettato su un computer. Queste tecnologie di “ingegneria biologica” hanno reso reale uno dei sogni dei pionieri delle nanotecnologie, vale a dire il dispiegamento di assemblatori molecolari in grado di costruire qualsiasi forma con precisione atomica, seguendo un design razionale.
Ciò che è interessante qui è che la storia non si è svolta esattamente come immaginavano i pionieri della nanotecnologia o come “prevedevano” le prime visioni dei “nanorobot” perché questa nanotecnologia non emerge più da un punto di vista riduzionista che prevede nanomacchine totalmente artificiali dispiegate all’interno di cellule viventi. Invece, utilizza la natura stessa, sfruttando la sua complessità e la sua storia evolutiva per creare nanostrutture. Ispirato dalla natura, questo nuovo approccio alla formazione della materia starebbe già producendo scoperte sorprendenti nel campo della medicina, come, ad esempio, strutture progettate simili a virus. Tale approccio ha il potenziale per evolversi e rivoluzionare il modo in cui l’industria farmaceutica crea i vaccini e cura i tumori.
Questo stesso approccio, ispirato alla complessità della natura e alla sua storia evolutiva, viene ora applicato alla progettazione di nuovi antibiotici in grado di superare la resistenza batterica. La maggior parte degli antibiotici sono piccole molecole che si legano a molecole batteriche per ucciderle o impedirne la crescita, ma i batteri possono facilmente mutare per creare difese chimiche che liberano dall’antibiotico. Appena nel dicembre 2019, una collaborazione nel Regno Unito tra fisici, nanotecnologi, biofisici, biologi, ricercatori biomedici e informatici, guidata da Maxim G Ryadnov del National Physical Laboratory, ha riportato sulla rivista ACS Nano8 di aver costruito un nano-icosaedro utilizzando bit di proteine presenti nel nostro sistema immunitario il quale potrebbe uccidere i batteri in modo molto efficiente. Il team è stato ispirato dal modo in cui i virus (come nel nostro sistema immunitario innato) uccidono i batteri creando nano-fori nella loro superficie, usando la fisica piuttosto che la chimica. Il nano-icosaedro che hanno progettato utilizza la carica elettrica e l’idro-fobicità per attaccarsi e distruggere i batteri, e lo fa così velocemente che i batteri non possono eguagliare la sua velocità nell’evoluzione della resistenza ad essi.
Il successo dell’approccio di Ryadnov si basa su una combinazione di abilità: comprensione della struttura delle proteine e della fisica dell’assemblaggio delle proteine, familiarità con la biologia di batteri e virus e tecniche biomediche necessarie per valutare l’efficacia degli antibiotici, con simulazioni computazionali e tecniche di microscopia prese dalla fisica. Indica, ugualmente, la via da seguire per un futuro in cui gli studiosi possano “adottare” strategie evolutive, sviluppate nel tempo nel nostro sistema immunitario, per superare i problemi medici ingegnerizzando nuove versioni di tali strategie su scala nanometrica.
Approcci simili hanno già avuto successo commerciale in campi lontani dalla medicina, come quello dell’elettronica. Un ottimo esempio è quello costituito dalla società biotech californiana Zymergen. Con l’aiuto dell’informatica avanzata e dell’intelligenza artificiale, Zymergen ingegnerizza i microbi (lieviti e batteri) per produrre molecole che non possono essere prodotte da aziende farmaceutiche o chimiche tradizionali specializzate in applicazioni mediche. Ma la portata di Zymergen va oltre la medicina: utilizzando una combinazione di biologia, intelligenza artificiale, informatica e nanotecnologie all’avanguardia, l’azienda ha creato i materiali più avanzati necessari per l’industria della telefonia mobile. Infatti, a febbraio scorso, Samsung ha presentato un nuovo modello di telefono cellulare con uno schermo pieghevole. L’ostacolo principale alla creazione di un dispositivo di questo tipo è stato trovare materiali in grado di corrispondere al meglio in termini di qualità dell’immagine, essendo allo stesso tempo flessibili e suscettibili di piegarsi e dispiegarsi migliaia, forse anche milioni di volte durante la vita del telefono. Zymergen ha dimostrato che tali materiali high-tech sono meglio costruiti utilizzando bio-fattorie progettate al computer che producono su scala nanometrica.
Ciò verso cui la nuova nanotecnologia sembra puntare è un inesorabile oscuramento dei confini tra le scienze. Sebbene ancora in uno stato embrionale, la nuova scienza transmateriale per la produzione di materiali artificiali, ispirata alla complessità e alla storia evolutiva in biologia, è già utilizzata per creare nuovi farmaci, sviluppare nuove strategie per la rigenerazione di tessuti e organi e migliorare le risposte del sistema immunitario. Parallelamente, i dispositivi bio-inorganici ibridi che imitano i processi biologici saranno presto utilizzati nei nuovi computer e dispositivi elettronici. Raffinando sempre più la loro capacità di apprendere dalla complessità e dalla storia evolutiva in biologia adoperando i metodi della fisica, i nano-tecnologi starebbero sbarazzandosi del giogo del riduzionismo e imparano a distillare le ricette dell’Universo per fabbricare e assemblare la materia dalla scala nanometrica. Nel processo, sostengono gli addetti, i nano-tecnologi starebbero rivoluzionando la tecnologia e la medicina. Come abbiamo, però, già accennato, le aspettative non sono state all’altezza del clamore. Come a novembre del 2019 segnalavano Vinay Bhardwaj, Ajeet Kaushik, Ziad M. Khatib, Madhavan Nair e Anthony J. McGoron al momento meno di 20 nanomedicine erano state approvate per l’uso nel trattamento del cancro. La ricerca di proiettili magici e di scorciatoie fortunate per curare le malattie della nanotecnologia, perfino quando cerca di prestare attenzione alla complessità della biologia coinvolta, non si è ancora dimostrata particolarmente fertile. Infatti, come segnala la stessa Sonia Contera, rispecchiando le strategie della farmacologia, la nanomedicina ha, fino ad oggi, largamente riprodotto i suoi fallimenti.
Immagini generate con Adobe Firefly
______________Note _________________
1 Sonia Contera. Nano Comes to Life: How Nanotechnology Is Transforming Medicine and the Future of Biology. Princeton University Press, 2019
2 Il buckminsterfulleren (nome IUPAC (C60-Ih)[5,6]fullerene) è il più piccolo fullerene nel quale due pentagoni non condividono un lato. Fu scoperto il 4 settembre 1985. I fullereni costituiscono una classe di sostanze allotrope molecolari del carbonio. Le molecole di fullerene, costituite interamente di carbonio, assumono una forma simile a una sfera cava, a un ellissoide o a un tubolare. I fullereni di forma simile a una sfera o a un ellissoide sono chiamati buckyball mentre quelli di forma tubolare sono chiamati buckytube o nanotubi di carbonio. I fullereni sono strutturalmente simili alla grafite costituita di anelli esagonali collegati tra loro su un piano, ma si differenziano per alcuni anelli di forma pentagonale o a volte ettagonale che impediscono una struttura planare. La struttura planare, costituita esclusivamente da anelli esagonali, è invece detta grafene. Il più piccolo e il più diffuso fullerene in cui nessuna coppia di pentagoni condivide un bordo, poiché questa condivisione risulterebbe destabilizzante, è il buckminsterfullerene. La struttura del buckminsterfullerene è quella di un icosaedro troncato costituito da esagoni e pentagoni, come un pallone da calcio, ai cui vertici si trova un atomo di carbonio e i cui bordi rappresentano i legami. Il nome di questo fullerene fa riferimento alla somiglianza con le cupole geodetiche predilette dall’architetto Richard Buckminster Fuller.
3 Junghuei Chen & Nadrian C. Seemanns. Synthesis from DNA of a molecule with the connectivity of a cube. In “Nature”, Vol. 350, pages 631-633, 1991
4 Il grey goo (alternativamente scritto gray goo, letteralmente “poltiglia grigia” o “sostanza appiccicosa grigia”) è un ipotetico scenario apocalittico in cui la fine del mondo è provocata dalla nanotecnologia molecolare, dove dei robot fuori controllo e autoreplicanti consumano tutta la materia del pianeta mentre si riproducono moltiplicandosi, uno scenario noto come ecofagia (“che divora l’ambiente”). Le macchine autoreplicanti di tipo macroscopico sono state originariamente descritte dal matematico John von Neumann e sono a volte indicate come macchine von Neumann. Il termine grey goo venne coniato dal pioniere della nanotecnologia Eric Drexler nel suo libro del 1986 Engines of Creation e l’idea fu resa popolare per la prima volta verso la fine dello stesso anno nelle pagine della diffusa rivista Omni.
5 Un cristallo colloidale è un aggregato ordinato di particelle, analogo a un cristallo standard le cui sottounità che si ripetono sono atomi o molecole.
6 C. Lee Ventola. The Antibiotic Resistance Crisis. Part 1: Causes and Threats. In “Pharmacy & Therapeutics”, 40 (4): 277-283, 2015
7 In chimica, le proteine (o protidi) sono macromolecole biologiche costituite da catene di amminoacidi legati uno all’altro da un legame peptidico (ovvero un legame tra il gruppo amminico di un amminoacido e il gruppo carbossilico dell’altro amminoacido, creato attraverso una reazione di condensazione con perdita di una molecola d’acqua). Le proteine svolgono una vasta gamma di funzioni all’interno degli organismi viventi, tra cui la catalisi delle reazioni metaboliche, funzione di sintesi come replicazione del DNA, la risposta agli stimoli e il trasporto di molecole da un luogo ad un altro. Le proteine differiscono l’una dall’altra soprattutto nella loro sequenza di amminoacidi, la quale è dettata dalla sequenza nucleotidica conservata nei geni e che di solito si traduce in un ripiegamento proteico e in una struttura tridimensionale specifica che determina la sua attività. In analogia con altre macromolecole biologiche come i polisaccaridi e gli acidi nucleici, le proteine costituiscono una parte essenziale degli organismi viventi e partecipano praticamente in ogni processo che avviene all’interno delle cellule. Molte fanno parte della categoria degli enzimi, la cui funzione è catalizzare le reazioni biochimiche vitali per il metabolismo degli organismi. Le proteine hanno anche funzioni strutturali o meccaniche, come l’actina e la miosina nei muscoli e le proteine che costituiscono il citoscheletro, che formano una struttura che permette di mantenere la forma della cellula. Altre sono fondamentali per la trasmissione di segnali inter ed intracellulari, nella risposta immunitaria, per l’adesione cellulare e per il ciclo cellulare. Le proteine sono elementi necessari anche nell’alimentazione degli animali, dal momento che essi non possono sintetizzare tutti gli amminoacidi di cui hanno bisogno e devono ottenere quelli essenziali attraverso il cibo. Grazie al processo della digestione, gli animali scindono le proteine ingerite nei singoli amminoacidi, che poi vengono utilizzati nel metabolismo.
8 Ibolya E. Kepiro, Irene Marzuoli, Katharine Hammond, Xiaoliang Ba, Helen Lewis, Michael Shaw, Smita B. Gunnoo, Emiliana De Santis, Urszula Łapinska, Stefano Pagliara, Mark A. Holmes, Christian D. Lorenz, Bart W. Hoogenboom, Franca Fraternali, and Maxim G. Ryadnov. Engineering Chirally Blind Protein Pseudocapsids into Antibacterial Persisters. In “ACS Nano”, 14, 1609−1622, 2020